10.5 Kupfergewinnung
Während unseres Besuchs erhielten wir Einblicke in die Kupfergewinnung der Minen Chuquicamata und Mina Sur. Ihre Aufbereitungswege sind in Abb. 10.5.1 schematisch dargestellt. Da in Chuquicamata die oxidischen Kupfererze bis auf kleine Reste im Nordteil des Tagesbaues abgebaut sind, wird das Kupfer dort ausschließlich aus sulfidischen Erzen (z.B. CuFeS2 – Chalkopyrit/Kupferkies) gewonnen. In Mina Sur hingegen wird hauptsächlich oxidisches Erz (z.B. Cu2O – Cuprit/Rotkupfererz) abgebaut, weshalb sich die Aufbereitungsverfahren deutlich unterscheiden.
Chuquicamata: Pyrometallurgisches Verfahren
Nach der Sprengung wird das gebrochene Gestein zunächst in einem Crusher zerkleinert. Damit der ineffiziente Transport durch Muldenkipper so kurz wie möglich gehalten wird, befindet sich der Primary Crusher bereits auf halber Höhe am Südrand der Grube. Da dessen Kapazität von etwa 105000 t/d nicht zur Bewältigung des angelieferten Roherzes ausreicht, befindet sich am Grubenrand ein weiteres Gerät, der Secondary Crusher. Um den weiteren Aufbereitungsprozess ohne Unterbrechungen betreiben zu können, wird das Gestein zunächst im Dome zwischengelagert.
Im Concentrator wird das Gestein bis auf 300 µm gemahlen und einer ersten Flotation unterzogen. Unter Zusatz von Wasser kommt es dabei aufgrund der unterschiedlichen Benetzbarkeit von Metallsulfiden / –oxiden und Silikaten zur Trennung von Erz und tauben Gestein. Eine weitere Flotation trennt Kupfer von Molybdän, indem durch Zugabe von Chemikalien Kupfer an Luftblasen gebunden wird und in Form von Schaum abgeschöpft werden kann. Im Zuge der anschließenden Trocknung wird das entzogene Wasser aufgefangen, gereinigt und recycelt (Wirkungsgrad 99%).
Bei der Weiterverarbeitung wird das sulfidische Konzentrat im Smelter aufgeschmolzen, wodurch Verunreinigungen als Schlacke aufschwimmen und das gereinigte Eisen-Kupfer-Sulfid (Kupferstein) als Bodensatz absinkt. In einem weiteren Schritt wird der Kupferstein unter Zusatz von Kalk geröstet, Eisensulfid zu Eisenoxid oxidiert und durch Zugabe von Quarz als Schlacke abgetrennt. Freiwerdendes Schwefeldioxid (SO2) wird aufgefangen und zu Schwefelsäure (H2SO4) aufbereitet, um es im hydrometallurgischen Verfahren zu verwenden oder zu verkaufen.
Anschließend wird im Converter ein Teil des gewonnenen Kupfersulfides (Cu2S – Chalkosin/Kupferglanz) mit reinem Sauerstoff bei 1300°C zu Kupferoxid (Cu2O – Cuprit/Rotkupfererz) oxidiert (1), um sich mit dem verbleibenden Kupfersulfid zum sogenannten Garkupfer umzusetzen (2), aus dem Anoden mit einem Kupfergehalt von 99,7 % zu je 420 kg gegossen werden.
2 Cu2S + 3 O2 -> 2Cu2O + 2 SO2 (1)
2 Cu2O + Cu2S -> 6 Cu + SO2 (2)
Da für viele elektronische Anwendungen ein höherer Reinheitsgrad benötigt wird, der sich mit chemischen Verfahren nicht erreichen lässt, wird Garkupfer mittels Elektrolyse in 99,9 % reines Kupfer umgewandelt. Dabei wird an bis zu 100 hintereinandergeschalteten Kupferanoden eine Spannung von 0,4-1,0 V angelegt, so dass Kupfer und unedlere Metalle, wie z.B. Zinn, oxidiert werden und unter langsamer Auflösung der Anode in Lösung gehen. Gelöste Metallionen setzen sich selektiv an der Kathode ab und bilden dort hochreine Kupferplatten. Die edleren Metalle (Gold, Silber etc.) werden aufgrund ihres höheren Normalpotentials nicht oxidiert, gehen somit auch nicht in Lösung, sondern fallen als sogenannter Anodenschlamm zu Boden, der als wertvolles Nebenprodukt gewonnen wird.
Mina Sur: Hydrometallurgisches Verfahren
Wie auch in Chuquicamata wird das gesprengte Gestein auf möglichst kurzen Wegen einem Crusher zugeführt, von dem aus es zur Zwischenlagerung in einen Dome gebracht wird.
Die Extraktion des Kupfers erfolgt danach durch Laugung. Dazu wird das zerkleinerte Gestein etwa 100 Tage auf riesigen Halden gelagert und regelmäßig mit Schwefelsäure durchtränkt, was zur Bildung von gut wasserlöslichem Kupfersulfat (CuSO4) (3) führt, welches in Lösung am Grund der Halde aufgefangen wird. Das zunehmend häufiger angewandte Bioleaching-Verfahren benutzt dagegen die bakteriell vermittelte Oxidation von Sulfiden und leicht löslichen Sulfaten. Die so gebildeten Lösungen werden der Elektrolyse zugeführt.
Cu2O + 2 H2SO4 + 0,5 O2 -> 2 CuSO4 + 2 H2O (3)
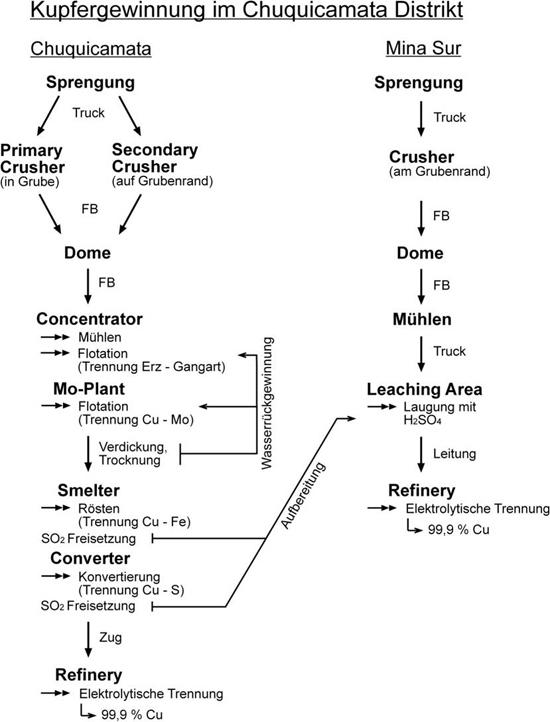
Abb. 10.5.1: Flussdiagramm zur Kupfergewinnung im Chuquicamata-Distrikt vom Ausgangsgestein bis zum 99,9% reinen Kupfer; FB = Förderband. Abbildung: D. Müller.